유전자 치료는 암에 대해 큰 효과를 보지 못하고 있는 기존 방법의 대안 치료법으로 유전자에 문제가 있기 때문에 생겨나는 암세포를 유전자 단계부터 치료하는 개념이다.
이런 근본적인 단계로부터의 유전자 치료 연구 방향 중에 하나인 RNA 간섭 (RNA interference)은 현재 가장 효과적인 방법으로 인정돼 많은 연구가 진행되고 있다.
명지대 박노경 교수 연구팀은 유전자 이상에 의한 질병 치료에 적용할 특정 유전자의 발현을 억제하는 나노반응체 합성 기술을 개발해 바이오․의학 분야에 다양하게 적용할 수 있을 것으로 보인다.
질병을 유전자 단계에서 치료하는 RNA 간섭은 짧은 길이의 RNA가 자신과 상보적인 RNA에 결합해 잘못된 단백질을 생성하지 못하도록 방해하는 방법이나 이때 활용되는 작은 간섭 RNA는 불안정하고 세포 내부로 주입되기 쉽지 않아 효율이 낮은 한계점이 있다.
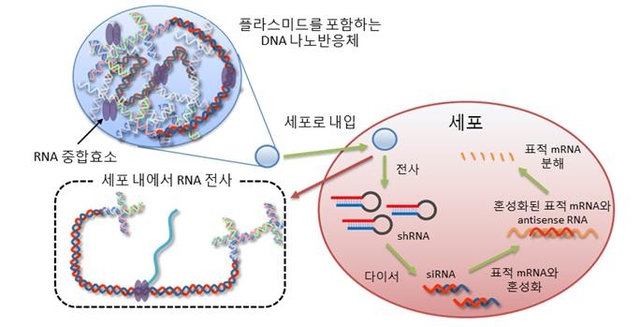
연구팀은 초소형 공장과 같이 생체 내에서 작은 간섭 RNA를 생산하는 나노반응체를 개발했다.
그 결과 작은 간섭 RNA의 생성이 8배 이상 증가했고, 작은 간섭 RNA가 표적으로 삼은 단백질의 생성을 억제하는 효과는 5배 이상 증가했다.
RNA 간섭 정도를 검증하기 위해 비교적 형광을 통한 정성 및 정량 분석이 쉬운 녹색 형광 단백질(GFP, green fluorescence protein)을 만들어내는 유전자를 표적으로 삼았다.
나노반응체의 검증을 위해 RT-qPCR (real time quantitative polymerase chain reaction)을 이용했다.
이것은 만들어진 RNA 서열을 증폭이 용이한 DNA로 역전사한 뒤에 PCR 반응을 통해 수백 만에서 수십 억 배 증폭하여 정량하는 방법인데 이것을 이용하면 분석 용액 상에 단 한 가닥의 RNA만 존재하더라도 정량적으로 검출 할 수 있다.
이 분석 방법을 통해 나노반응체에서 만들어진 짧은 간섭 RNA가 일반적인 플라스미드보다 더 많이 만들어지는 것을 확인하였고 GFP mRNA를 더 많이 억제한다는 것을 확인했다.
살아 있는 세포 수준에서도 나노반응체의 높은 RNA 간섭 효과를 확인하기 위해, GFP를 생산할 수 있는 유전자를 가지는 포유류 세포 (MDCK cell)에 나노반응체를 처리하고 다른 다양한 대조군들과 비교했다.
형광을 이용한 다양한 분석 방법들 외에도 세포 내부에서 발현하는 RNA를 추출하여 RT-qPCR을 통해 정량 분석한 결과, 다양한 대조군에 비해 효과적인 RNA 간섭 효과를 확인할 수 있었다.
특히 작은 간섭 RNA를 생산 가능한 유전자를 가진 플라스미드를 DNA 수화젤에 접목시켜 높은 효율을 가지고 긴 시간 안정적으로 간섭 RNA를 만들 수 있는 DNA 수화젤 합성과 동시에 여러 분석을 통해 더 높은 RNA 간섭 효과를 나타냄을 확인했다.
개발된 나노반응체는 DNA 수화젤에 플라스미드 DNA가 연결된 형태이다.
RNA나 플라스미드 DNA 상태로 주입하는 것에 비해 세포 내로 전달이 용이하고, 작은 간섭 RNA 생성이 효율적이다.

박노경 교수는 “생체 내에서 RNA나 단백질 등을 자유자제로 생산할 수 있게 될 것”이라며 “플라스미드 DNA에 삽입되는 유전자의 종류를 바꿈으로서 바이오․의학 분야에 다양하게 적용될 수 있을 것”이라고 설명했다.
이 연구는 결과는 국제학술지 네이처 커뮤니케이션즈(Nature Communications)에 10월 18일 게재됐다.
(논문명 : A RNA producing DNA hydrogel as a platform for a high performance RNA interference system)



전체댓글 0