국내 연구진이 암의 발생과 전이를 억제할 수 있는 새로운 작동경로를 최초로 규명했다. 22일 포항공대(POSTECH.포스텍)에 따르면 화학과 임현석 교수, 이영주 박사 연구팀이 암 세포 안의 표적 단백질만 골라 효율적으로 분해할 수 있는 단백질 분해제 개발에 성공했다.
이 연구결과는 화학분야 권위지인 독일화학회지 ‘앙게반테 케미(Angewandte Chemie)’에 게재됐으며, 10% 미만의 논문에만 주어지는 ‘주목받는 논문’으로 선정됐다.
N-말단 분해 경로(N-degron pathway)는 단백질의 N-말단에 위치하는 잔기(residue)가 그 종류나 상태에 따라 분해신호(N-degron)로 작용하고, N-말단 분해 신호 수용체(N-recognin)가 이를 인식해 분해를 매개하는 단백질 조절경로이다.
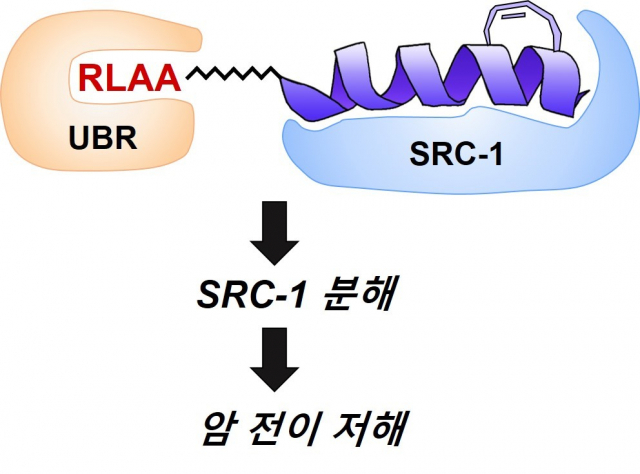
연구팀은 비정상적인 스테로이드 수용체 보조 활성화제-1(SRC-1)를 분해하는 ‘단백질 분해 표적 키메라(PROTAC, proteolysis targeting chimera)’를 합성했다. 이 화합물이 N-말단 분해 경로를 통해 세포 내 SRC-1의 분해만을 유도함을 확인했다.
또한, 생물체의 세포질 내에 존재하는 상당수의 단백질이 N-말단 경로에 의해 분해되기 때문에, 연구팀이 개발한 N-말단 기반의 PROTAC을 이용하면 세포의 유형에 관계없이 단백질을 효과적으로 분해할 수 있음을 발견했다. 또 암 세포의 전이 활성(침윤과 이동)도 억제하는 것을 확인했다.

논문의 제1저자인 이영주 박사는 ”암 전이에 매우 중요한 역할을 하는 SRC-1을 효과적으로 억제하는 화합물을 개발했다“며 ”특히, N-데그론을 이용한 단백질 분해 전략은 더 다양한 질환에서 적용이 가능할 것으로 기대된다“고 말했다.
임현석 교수는 “이 기술을 이용하면 기존의 신약개발 방법으로는 접근할 수 없었던 치매, 암 등 난치성 질환 관련 단백질을 약물 표적으로 이용할 수 있다” 며 “이는 현재는 존재하지 않는 질병의 치료제 개발도 앞당길 수 있을 것”이라며 기대감을 나타냈다.
한편, 이번 연구는 고려대 송현규 교수, 서울대 안지완 교수, KIST 이준석 박사가 함께 참여했으며, 과학기술정보통신부와 보건복지부가 주관하는 인공지능 신약개발 플랫폼 구축사업과 한국연구재단 중견연구자지원사업의 지원을 받아 수행됐다.




전체댓글 0